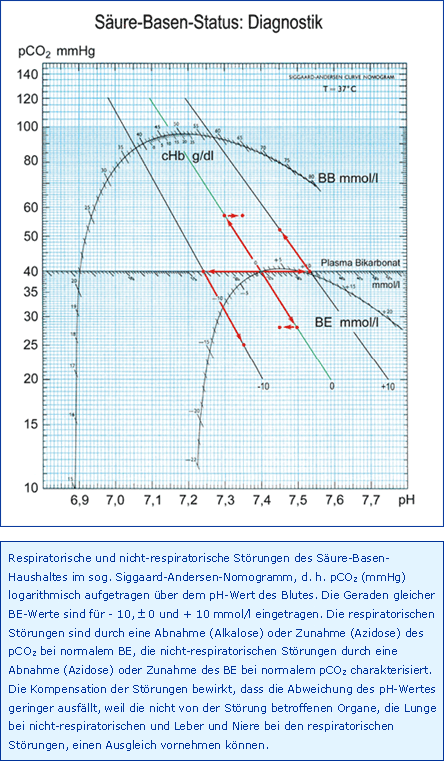
Diagnostik
Säure-Basen-Status
Unter dem Säure-Basen-Status versteht man die Summe derjenigen Mess- und Rechengrößen, die eine Diagnostik der Störungen des Säure-Basen-Haushaltes ermöglichen.
Dazu gehören die Messwerte im Plasma für den pH, den Kohlendioxid-Partialdruck pCO2 (mmHg) und den Sauerstoff-Partialdruck pO2 (mmHg) sowie die Hämoglobin-Konzentration cHb (g/dl). Zusätzlich berechnet werden aus diesen Werten üblicherweise die sogenannte partielle O2-Sättigung psO2 (%) und der Base Excess BE (mmol/l) des Blutes.
Messwerte des Säure-Basen-Status
Der pH-Wert des Blutplasmas zeigt an, ob das Gleichgewicht zwischen CO2-Bildung und -Elimination sowie H+-Bildung und -Elimination im Normbereich liegt, ein pH von 7,40 gilt als Normwert. Der pCO2 des Blutes beschreibt eine normale oder gestörte CO2-Elimination über die Lunge. Ein pCO2 von 40 mmHg gilt als normal, eine Abweichung davon ist typisch für eine respiratorische Störung des Säure-Basen-Status, also der Lungenfunktion oder Beatmung.
Der BE des Blutes schließlich charakterisiert die nicht-respiratorische Seite des Säure-Basen-Status, der Normalwert beträgt 0 mmol/l.
Wie bereits erwähnt, werden die drei Messwerte pH, pCO2 und pO2 mit Elektroden erfasst, die im Plasma zu liegen kommen. Die Messung der Plasma-Werte zeigt deshalb eine gute Präzision, weil alle drei Werte im Kontakt mit den Erythrozyten erhoben werden, die für eine Pufferung sorgen: Der pH-Wert, der von der hohen Pufferkapazität des Plasma-HCO3- und Erythrozyten-Hämoglobins stabilisiert wird, der pCO2, der den Druck des physikalisch gelösten CO2 beschreibt, das im Gleichgewicht mit einer sehr hohen HCO3--Konzentration steht, und der pO2, der dem Druck des physikalisch gelösten O2 entspricht, der optimal aus dem großen O2-Pool der chemischen Bindung des Hämoglobins im Erythrozyten gespeist wird.
Fehlermöglichkeiten
Intra-analytische Fehler sind in den meisten Fällen auf eine mangelhafte Kalibrierung der Elektroden zurückzuführen. Da praktisch alle Hersteller von Blutgasanalysatoren vor einigen Jahren die weltweit akzeptierten Phosphatpuffer (pH 6,841 und 7,383) für die Kalibrierung der pH-Elektroden durch Hepes-Puffer eigener Rezeptur ersetzt haben, weisen pH-Elektroden einzelner Hersteller bisweilen Probleme bei der Präzision des zu messenden Blut-pH-Wertes auf. Die von jedem Hersteller für seine Geräte angebotenen wässrigen Kontrollmaterialien in Ampullen zur internen Qualitätskontrolle weisen nach wie vor einige Probleme auf, die sich an den großzügigen Zielwert-Bereichen ablesen lassen.
Für den Base Excess (BE, mmol/l), der nur rechnerisch aus beiden Messwerten erhalten wird, werden allerdings keine Zielwert-Bereiche angegeben. Diese schwanken im ungünstigsten Falle, d. h. wenn nach Herstellerangaben gerade noch zulässige pH- bzw. pCO2-Werte gemessen werden und der BE daraus berechnet wird, je nach Hersteller zwischen 4,9 und 8,0 mmol/l (Level 2, Normalwerte) [Zander 1995 (C)].
Berechnete Werte des Säure-Basen-Status
Ein traditionell schon immer vom Blutgasanalysator berechneter Wert ist die O2-Sättigung der Blutprobe, genaugenommen die partielle O2-Sättigung (psO2, %), leider auch funktionelle Sättigung genannt. Darunter wird der prozentuale Anteil des oxygenierten Hämoglobins an der Summe von oxygeniertem plus desoxygeniertem Hämoglobin verstanden. Dazu wird im Rechner des Gerätes aus dem pO2 und einer aktuellen O2-Bindungskurve (pH, pCO2, BE) der Blutprobe die psO2 berechnet, die ihrerseits für die Berechnung des BE benötigt wird.
Da dieser berechnete Wert bezüglich seiner Präzision anderen Verfahren deutlich unterlegen ist, zum Beispiel auch der mit einem Pulsoxymeter gemessenen partiellen O2-Sättigung, sollte er keine weitere diagnostische Verwendung mehr finden und nur noch zur BE-Berechnung verwendet werden.
Der wichtigste berechnete Wert, aus pH, pCO2 (mmHg) und cHb (g/dl) ermittelt, ist der Base Excess BE in mmol/l (Abb. Base Excess). Er gibt an, wie viel mmol/l an H+ oder OH- nötig wären, den pH-Wert des Blutes bei pCO2 40 mmHg auf 7,40 zu normalisieren. Während bei älteren Geräten die cHb eingegeben werden musste, wird diese heute meistens direkt gemessen.
Definitionsgemäß muss der BE bei rein respiratorischen Störungen des Säure-Basen-Status unverändert 0 mmol/l betragen, auch wenn sich der pCO2 und nachfolgend der pH deutlich ändern, z. B. im Sinne einer respiratorischen Azidose (pCO2 ↓, pH ↓) oder Alkalose (pCO2 ↓, pH ↓).
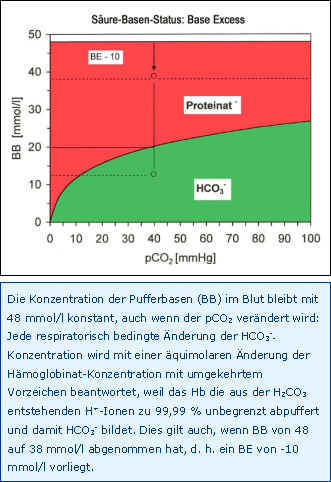
Hingegen sind nicht-respiratorische Störungen definitionsgemäß durch einen veränderten BE mit normalem pCO2 charakterisiert, solange sie nicht kompensiert sind. Damit ist der BE, neben dem sogenannten Standard-Bikarbonat, die klassische nicht-respiratorische Größe des Säure-Basen-Status, die ursprünglich nomographisch, heute rechnerisch ermittelt wird. Entscheidend aber ist, dass der BE diejenige klinische Größe ist, die für eine mögliche therapeutische Korrektur aller nicht-respiratorischen Störungen des Säure-Basen-Haushaltes benutzt wird.
Trotz unterschiedlicher Berechnungsformeln für den BE differieren die BE-Werte zwischen den wichtigsten Herstellern von Blutgasanalysatoren nur unwesentlich um ca. 1 mmol/l. Während allgemein akzeptiert ist, dass sich der BE bei respiratorischer Änderung des pCO2 und daraus resultierender Änderung des pH definitionsgemäß nicht ändern darf, ist diese Frage für eine Änderung des O2-Partialdruckes bzw. der O2-Sättigung und daraus resultierender Änderung des pH in der ursprünglichen Literatur sowie zwischen den verschiedenen Herstellern von Blutgas-Analysatoren strittig.
Wird nämlich eine Blutprobe bei pCO2 = 40 mmHg und psO2 = 96 % vollständig desoxygeniert (psO2 = 0 %), so steigt der pH-Wert von 7,40 auf etwa 7,44 an. Für diese Blutprobe, die definitionsgemäß einen BE von 0 mmol/l aufweisen muss, werden derzeit von verschiedenen Geräten Werte zwischen - 1,1 und + 5,7 mmol/l angegeben. Über diese Diskrepanzen informiert, haben die meisten Hersteller von Blutgasanalysatoren angekündigt, die BE-Berechnungen zu verbessern. Kompliziert wird die Situation dadurch, dass verschiedene Geräte für beide BE-Berechnungen unterschiedliche Bezeichnungen verwenden (z. B. BE in vivo versus BE in vitro), was aus den jeweiligen Betriebsanleitungen nicht eindeutig hervorgeht. Es ist zu hoffen, dass sich diese Situation wie folgt verbessern wird [Zander 1995 (C)]:
Die richtige Berechnung des BE unter Berücksichtigung der vorhandenen O2-Sättigung stellt sicher, dass ein Blutgasanalysator nur einen BE ermittelt und anzeigt, der für jede arterielle, gemischt-venöse und venöse Blutprobe erhalten werden kann.
Anders formuliert: Der BE des venösen Blutes (vor der Lunge) muss per definitionem identisch sein mit dem des arteriellen Blutes (nach der Lunge), da der BE unabhängig von den respiratorischen Größen pCO2 und pO2 sein muss. Der entscheidende Vorteil, nämlich Verzicht auf eine arterielle Blutentnahme zur Bestimmung des BE, wird später nochmals aufgegriffen werden.
Auch wenn die Hersteller von Blutgasanalysegeräten bisweilen eine Vielzahl zusätzlicher Parameter anbieten, deren theoretischer Hintergrund fraglich und ihr therapeutischer Nutzen deshalb meistens zu vernachlässigen ist, sollten für den klinischen Alltag möglichst einfache Messwerte für Diagnostik und Therapie erhoben werden.
Praktisch überflüssig ist zum Beispiel die Berechnung eines BE der Extrazellularflüssigkeit mit einer fiktiven cHb von 5 g/dl, auch wenn er sich für den Fall der respiratorischen Azidose gut begründen lässt: Ein Anstieg des pCO2 führt in vivo im proteinarmen Extrazellularraum zu einer anderen pH- und damit BE-Änderung als unter in vitro Bedingungen im Blut. Der mögliche therapeutische Vorteil konnte nicht genutzt werden, weil die Therapie einer respiratorischen Azidose nicht über eine Änderung des BE erfolgt. Der berechnete Wert des Standard-Bikarbonats (cHCO3-, mmol/l), d. h. derjenigen cHCO3- im Plasma, wie sie bei einem physiologischen pCO2 von 40 mmHg (eine mögliche respiratorische Komponente wurde rechnerisch beseitigt) zu erhalten wäre, hat prinzipiell die gleiche Bedeutung als nicht-respiratorische Größe des Säure-Basen-Status wie der BE: Bei einem rechnerisch "künstlich" hergestellten pCO2 von 40 mmHg, d. h. "respiratorisch normal", muss das Blutplasma bei einem BE von 0 mmol/l eine cHCO3- von 24 mmol/l aufweisen. Abweichungen hiervon beschreiben nicht-respiratorische Störungen. Da keine Vorteile gegenüber dem BE zu erkennen sind, hat sich diese Größe nicht durchsetzen können. Die Einheiten aber sind unterschiedlich: Standard-HCO3- in mmol/l Plasma und BE in mmol/l Blut.
Das gleiche gilt für die von einzelnen Geräten berechnete aktuelle cHCO3- des Plasmas, die sowohl auf respiratorische als auch nicht-respiratorische Änderungen reagieren muss: Eine Erhöhung des pCO2 führt ebenso wie eine Erhöhung des pH-Wertes zu einer Zunahme der cHCO3- und umgekehrt.
Beispiel: Eine nicht-respiratorische Azidose (pH 7,31 bei pCO2 40 mmHg und BE - 6 mmol/l) zeigt die gleiche Plasma cHCO3- von 20 mmol/l wie eine respiratorische Alkalose (pH 7,54 mit pCO2 24 mmHg und BE ± 0 mmol/l).
Würde die nicht-respiratorische Azidose durch Hyperventilation vollständig kompensiert (pH 7,40 bei pCO2 28 mmHg trotz persistierendem BE - 6 mmol/l), so würde sich die cHCO3- auf 17 mmol/l vermindern; würde die respiratorische Alkalose über eine renale HCO3--Ausscheidung vollständig kompensiert (pH 7,40 trotz persistierendem pCO2 von 24 mmol/l bei BE - 8 mmol/l), dann würde hier die cHCO3- auf 14,5 mmol/l abfallen. Es ist offensichtlich, dass diese Größe, wie auch das von manchen Geräten berechnete Gesamt-CO2 des Blutes (ml/dl), für die klinische Diagnostik ungeeignet ist, da diese Größen keine Differenzierung zwischen respiratorischer und nicht-respiratorischer Seite des Säure-Basen-Status zulassen.
Auch die Berechnung der Gesamt-Pufferbasen-Konzentration (BB) im Blut, d. h. die Summe aus Proteinat (vor allem Hämoglobinat) und Bikarbonat (HCO3- im Blut) mit einem Normalwert von 48 mmol/l, bringt für die klinische Praxis keine Vorteile. Zur Diagnostik des Säure-Basen-Status ist der Base Excess BE anderen berechneten Größen deutlich überlegen, so dem BE der Extrazellularflüssigkeit, der aktuellen Bikarbonat-Konzentration, dem Standard-Bikarbonat und der Konzentration der Gesamt-Pufferbasen.
Blutgewinnung
Grundsätzlich erfolgt die Diagnostik im arteriellen Blut, da auf diese Weise die Funktion des respiratorischen Regelorgans Lunge mitbeurteilt werden kann, was vor der Lunge, d. h. im venösen, zentralvenösen oder gemischt-venösen Blut, nicht möglich wäre.
Da einige Blutgasanalysatoren für die vollständige Diagnostik, nämlich Erweiterung vom alleinigen Säure-Basen-Status auch auf den Sauerstoff-, Elektrolyt- und Metabolit-Status, Probenvolumina bis zu 400 µl benötigen, wird unter klinischen Bedingungen sehr häufig ein bestehender arterieller Zugang zur Probengewinnung mit einer Spritze benutzt.
Als Alternative kommt die Punktion des Ohrläppchens in Frage, nachdem es mit einer lokalen Hyperämie (z. B. Finalgon®) vorbereitet wurde. Die lokale Hyperämie ist Voraussetzung dafür, dass in jedem Falle nur arterielles Blut gewonnen wird. Dazu muss allerdings die lokale Durchblutung (Hyperämie) soweit gesteigert werden, dass die arterio-venösen Differenzen für die entsprechenden Parameter (O2 und CO2) auf nahezu Null gebracht werden. Während Probenvolumina von 100 - 150 µl , d. h. 4 - 6 Tropfen Blut, ohne Schwierigkeiten mit einer heparinisierten Kapillare aus dem hyperämisierten Ohrläppchen gewonnen werden können, gilt dies für Volumina von zum Beispiel 400 µl nicht mehr.
Fehlermöglichkeiten
Prä-analytische Fehler entstehen zumeist durch mangelhafte Blutprobengewinnung und fehlerhafte Lagerung der Blutproben.
Jede noch so kleine Luftblase in der Kapillare oder Spritze muss zu einer Abnahme des pCO2 und Zunahme des pO2 führen, da es zu einer möglichen Äquilibrierung der Blutprobe mit dem pCO2 (0 mmHg) und dem pO2 (150 mmHg) der Luft kommen muss. Die Heparinisierung von Kapillaren und Spritzen hingegen verursacht heute praktisch keine Fehler mehr.
Während Glaskapillaren keine nennenswerten Änderungen der Gaspartialdrücke verursachen, gilt dies für Kunststoffsspritzen nicht. Paradoxerweise führen die meisten, speziell für Blutgasanalysen auf dem Markt angebotenen Spritzen zu deutlichen Abweichungen der Gaspartialdrücke insbesondere bei längerer Lagerungszeit zwischen Blutabnahme und Analyse im Blutgasanalysator. Die einfachsten 2 ml-Spritzen, die im klinischen Alltag verwendet werden, genügen den Anforderungen am ehesten.
Jede Lagerung einer Blutprobe über 10 - 15 min hinaus, sollte vermieden werden, da der Metabolismus von Erythrozyten und Leukozyten zu einer Abnahme des pO2 und einer Zunahme des pCO2 führt. Eine besondere Gefahr stellt die Sedimentation der Erythrozyten dar, die schon nach wenigen Minuten Lagerungszeit zu Fehlern führen kann.
Arterielles oder venöses Blut?
Die Frage, ob für die Ermittlung des Säure-Basen-Status mit einem Blutgasanalysator arterielles oder venöses Blut eingesetzt werden kann, hängt von der Größe des Probenvolumens, also Anzahl der beabsichtigten Bestimmungen, und von der Art des Messwertes ab.
Die reinen Säure-Basen-Status-Messungen, nämlich pH, pCO2 und pO2 erfordern eine arterielle Probengewinnung.
Bei strenger Indikation aber reduziert sich das Erfordernis einer arteriellen Blutproben-Entnahme allein auf die respiratorischen Messwerte pCO2 und pO2 zur Kontrolle der Lungenfunktion bzw. Beatmung des Patienten, während die nicht-respiratorische Seite, nämlich der BE, wie gezeigt aus jeder arteriellen oder venösen Blutprobe erfolgen kann. Somit könnte die Anzahl arterieller Punktionen erheblich reduziert werden.
Die Diagnostik des Säure-Basen-Status aus dem zentral-venösen oder besser gemischt-venösen Blut eines Pulmonalis-Katheters kann dann sinnvoll sein, wenn allein der - richtig berechnete - BE beurteilt werden soll. Ob die Beurteilung des pCO2 im gemischt-venösen Blut unter Notfallbedingungen bei Änderung des Herzminutenvolumens diagnostisch verwertbar ist, bleibt abzuwarten, da die Interpretation aufwendig sein dürfte.
Nicht-invasive Diagnostik des Säure-Basen-Status?
Die "blutige" Diagnostik des Säure-Basen-Status wird heute zum Teil auch "nicht blutig", d. h. nicht invasiv, ermöglicht, so dass eine diskontinuierliche durch eine kontinuierliche Überwachung des Patienten ersetzt werden kann.
Die kontinuierliche Messung des end-expiratorischen CO2-Partialdruckes (peECO2, engl. endtidal petCO2) mit modernen Anästhesiegas-Monitoren lässt beim spontan atmenden oder beatmeten Patienten eine indirekte Bestimmung des alveolären CO2-Partialdruckes (pACO2) mit einer Genauigkeit von 1 - 2 mmHg zu [Zander, Mertzlufft 1992 (A)], eine Genauigkeit, die für das arterielle Blut (paCO2) nicht immer erreicht wird. Da unter physiologischen Bedingungen die Differenz zwischen dem pACO2 und dem paCO2 (AaDCO2) nicht größer als 1 mmHg ist, können die drei Werte gleichgesetzt werden, nämlich: paCO2 = pACO2 = peECO2. Eine Überwachung des paCO2 mit sogenannten transkutanen Elektroden kann in diesem Zusammenhang für den Erwachsenen nicht empfohlen werden, da diese Methoden zu langsam und zu ungenau sind.
Die kontinuierliche Messung der partiellen arteriellen O2-Sättigung (psaO2, %) mit Pulsoxymetern erlaubt darüber hinaus eine einfache und genaue Kontrolle der Atmung oder Beatmung des Patienten, da sich eine gestörte Lungenfunktion eher in einer Änderung der psaO2 als des paCO2 äußern muss.
Die "blutige" Diagnostik des Säure-Basen-Status wird sich also in zunehmendem Maße auf die Bestimmung des Base Excess reduzieren, der aus den Messwerten pH, pCO2, pO2 und cHb einer arteriellen, gemischt-venösen oder venösen Blutprobe gewonnen werden kann.
Interpretation des Säure-Basen-Status
Keine der genannten Größen des Säure-Basen-Status erlaubt für sich allein eine sinnvolle Diagnostik, sondern nur die Kombination der Werte, wie dies in Tab. Primäre Störungen gezeigt wird.

Der pH-Wert allein hat praktisch keine diagnostische Aussagekraft, auch wenn er der Störung ihren Namen gibt. Vielmehr legen der pCO2 als die respiratorische Größe und der BE als die nicht-respiratorische Größe die Ursache der Störung fest und bestimmen die spätere Therapie.