
Forum 3 – Standardisierung des pH
(Ausgabe 10/2011)
Prinzipielle Vorbemerkungen
Die Tatsache, dass der pH einer Blut- oder Plasma-Probe den Gerinnungsstatus beeinflusst, wird weiterhin negiert: Im Vergleich zu 7,40 (100 %) beträgt die Gerinnungsaktivität beim pH von 7,2 nur noch ca. 50 % und beim pH von 7,60 immerhin fast 200 % [1].
Daraus ist zu folgern, dass der Gerinnungs-Diagnostik, je nach Verfahren, größere oder kleinere Fehler anhaften, wie die folgende Abbildung deutlich machen soll.
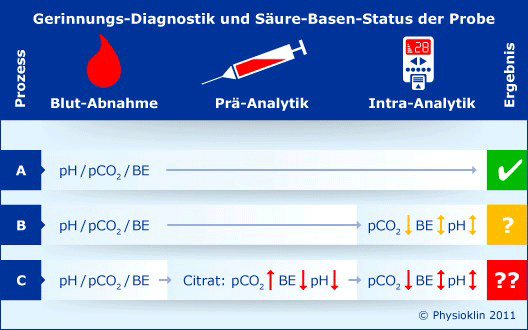
- In diesem - optimalen - Falle (A) würde der Säure-Basen-Status der zu untersuchenden Probe von der Abnahme bis zum diagnostischen Ergebnis unverändert bleiben. Dies wäre theoretisch mit POC-Verfahren möglich, wenn die Diagnostik direkt aus der Blutprobe erfolgt und die Reagenzien ohne weitere Zusätze appliziert würden.
- Bei diesen POC-Verfahren (B), vermutlich z.B. Coagucheck (Roche Diagnostics), I-STAT (Abbott) und Epoc (Alere), erfolgt die Diagnostik zwar direkt aus der Blutprobe, bei der Diagnostik werden aber - vermutlich - gepufferte Reagenzien eingesetzt, die den ursprünglichen pH-Wert verändern. Bei den hier als "Mini-Lab" bezeichneten Verfahren, wie z. B. Sonoclot (Sienco) und Multiplate (Verum Diagnostica, Instrumentation Laboratory) dürfte sich - vermutlich - der pH der Probe innerhalb des Gerätes unter der Diagnostik ändern, was es noch zu be- oder widerlegen gilt.
- In dieser Kategorie (C) finden sich auch "Mini-Labs" wie z. B. Rotem (Tem), TEG 5000 (Haemonetics) und PFA 100 (Siemens), die mit Citrat-Blut arbeiten und - vermutlich - zusätzlich gepufferte Reagenzien einsetzen. Die Verfahren des klassischen Gerinnungs-Labors fallen in die gleiche Kategorie, als Beispiele werden hier gepufferte Reagenzien von Instrumentation Laboratory, Siemens und Terumo beschrieben.
Gepufferte oder nicht gepufferte Citrat-Lösungen?
Das Forum 2 – Citratlösungen (Ausgabe 03/2011) hat mit einem geringfügig modifizierten Zitat geendet [2]: Die Konzentration, der Typ (gepuffert / ungepuffert), das Volumenverhältnis Citrat/Blut, der pH der Citratlösung und der Hämatokrit sind diejenigen präanalytischen Variablen, die den späteren Gerinnungstest besonders beeinflussen.
Hier wird der Aspekt gepufferte / nicht gepufferte Citrat-Lösungen genauer beschrieben. Üblicherweise werden Citrat-Lösungen, die neben dem Citrat auch noch Citronensäure enthalten, als gepuffert bezeichnet: Diese Lösungen stellen tatsächlich ein Puffersystem dar, das einen pH zwischen 5 und 6 stabilisieren kann. Da der pK3-Wert der Citronensäure (37 °C) aber 5,8 beträgt (pK1 3,0 und pK2 4,4) wird hier eine Pufferwirkung aufgebaut, die aber beim pH des Blut-Citrat-Gemisches von 7-8 nicht mehr wirksam wird.
Bei einer üblichen Verdünnung von 9 Teilen Blut plus 1 Teil Citrat-Lösung muss nun die Citronensäure vom Bicarbonat des Blutes gepuffert werden: Es entsteht eine metabolische Azdose mit negativem BE sowie eine große Menge CO2, die den pCO2 kräftig nach oben treibt. Das Resultat ist eine kombinierte metabolische plus respiratorische Azidose. Wie bereits gezeigt, resultieren dann pH-Werte von ca. 7,2 (gepuffert) und 7,4 (ungepuffert) [3].
Eine genauere Analyse liefern aktuelle Messwerte, die freundlicherweise von Herrn Prof. Dr. D. Fries (Abteilung Allgem. und Chirurg. Intensivmedizin) und Herrn Chr. Reif (Abteilung für Kinder- und Jugendheilkunde) der Medizinischen Universität Innsbruck erhoben und dankenswerter Weise zur Verfügung gestellt wurden.
Diese sind als Mittelwerte von 5 Probanden in der folgenden Tabelle aufgeführt, wobei 4 verschiedene Blutentnahme-Systeme mit ihren pH-Werten (Herstellerangaben) sowie zwei verschiedene Reagenzien-Sätze mit ihren pH-Werten (Herstellerangaben) geprüft wurden.
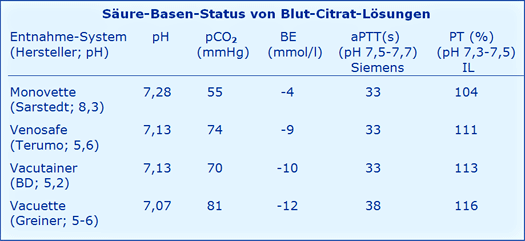
Die Ergebnisse können wie folgt interpretiert werden:
- Eine reine Citratlösung (Monovette) ohne nennenswerte Pufferkapazität ändert pH, pCO2 und BE des Blut-Citrat-Gemisches nur unwesentlich, der "normale" venöse pH von 7,35 mit pCO2 von 50 mmHg und BE von 0 mmol/l [5] bleibt, abgesehen von einer zu erwartenden, geringen Dilutions-Azidose, praktisch erhalten.
- So genannte gepufferte Citratlösungen (Gemisch aus Citrat + Citronensäure) erzeugen, je nach ihrem pH, einen negativen BE, einen erhöhten pCO2 (Umwandlung von HCO3 in CO2) und damit einen sehr niedrigen pH.
- Je niedriger der pH des Blut-Citrat-Gemisches desto länger fallen PT und aPTT aus, auch wenn die - unterschiedlich - gepufferten Reagenzien dies eigentlich verhindern sollen.
- Je höher der von der Citronensäure verursachte pCO2, desto instabiler die Lagerung.
Dieser letzte Punkt soll nochmals aufgegriffen werden, da er praktische Konsequenzen hat.
Das Ziel eines optimalen Blutentnahme-Systems sollte auch darin bestehen, ein Blut-Citrat-Gemisch in einer Spritze herzustellen, das für den Transport und die Lagerung möglichst stabile Verhältnisse besitzt.
Es wurde multizentrisch untersucht [4], ob die Zeit zwischen Blutabnahme und Messung, die Lagerungs-Temperatur und die mechanische Agitation zur Simulation eines Transportes Einfluss auf das Ergebnis des späteren Gerinnungstests haben. Die Autoren belegen, dass massive Unterschiede beim Testergebnis bei Variation der Lagerungszeit, der Temperatur sowie der Agitation resultieren. Insbesondere eine horizontale Agitation der Spritze führte zu einer stärkeren Gerinnungs-Aktivierung als eine vertikale. Im Gegensatz zur Interpretation der Autoren („we cannot explain this phenomenon“) ein plausibles Ergebnis, weil die Oberfläche zwischen Gasblase und Blut in horizontaler Position deutlich größer ist als in vertikaler Position, also der Gasaustausch im Sinne eines pCO2-Abfalls und pH-Anstiegs deutlich stärker ausfällt.
Die Aufforderung an die Hersteller von Blutentnahme-Systemen für Gerinnungs-Tests muss daher lauten, eine weitgehend gasdichte Blutgasspritze mit möglichst kleiner Gasblase sowie ungepuffertem Citrat für die Gerinnungs-Diagnostik in den Markt zu bringen.
Kommentar INSTAND e. V.
Die frühere Bezeichnung der 1966 gegründeten Fachgesellschaft, die sich seit 1968 Institut für Standardisierung und Dokumentation im medizinischen Laboratorium e. V. genannt hatte, hat sich gewandelt. Heute steht INSTAND e. V. für die Gesellschaft zur Förderung der Qualitätssicherung in medizinischen Laboratorien e. V. Der 1. Vorsitzende von INSTAND e.V. und zugleich Experte der Gerinnungsdiagnostik, Herr Prof. Dr. med. Michael Spannagl (LMU München, Klinikum Innenstadt, Medizinische Klinik, Hämostaseologie / Angiologie) hat 2010 und 2011 öffentlich bei den Mannheimer Transfusionsgesprächen der IAKH (Interdisziplinäre Arbeitsgemeinschaft für Klinische Hämotherapie) gepufferte Citratlösungen gefordert. Aus diesem Grunde wurde er um einen Kommentar zu der Frage gebeten, welche Art der Pufferung - aus seiner Sicht - für die Citratlösungen vorzuschlagen sei:
Wie soll gepuffert werden, welcher pH der Lösung und welcher Ziel-pH in der Mischung Blut / Citrat (9 + 1) ist anzustreben? Leider hüllt sich der 1. Vorsitzender von INSTAND e.V. - und damit auch INSTAND e. V. - seit Monaten in Schweigen.
Vor dem Hintergrund der publizierten Empfehlungen (s. Forum 2) aber ist eine Standardisierung dringend erforderlich:
Prä-Analytik
Clinical and Laboratory Standards Institute 2008:
Das für Gerinnungstests empfohlene Antikoagulans sollte 105-109 mmol/l, 3,13 % bis 3,2 % (üblicherweise als 3,2 % bezeichnet) des Dihydrats von Tri-Natrium-Citrat (Na3C6H5O7 ? 2 H2O) enthalten, gepuffert oder nicht gepuffert.
Polack et al. 2001 und Endler et al. 2010:
Das Citrat muss mit Citronensäure auf einen pH von 5,1-5,3 gepuffert werden, um den pH der Plasmaprobe zwischen 7,3 und 7,45 zu halten.
Endler et al. 2010: "Die internationale Gesellschaft für Thrombose und Hämostase (ISTH) empfiehlt für alle Gerinnungstests mit Hepes gepuffertes Zitrat."
Mitteilung bzw. Homepage Fa. Becton Dickinson 2011:
Gepuffertes Natriumzitrat, pH-Wert 5,5 bzw. gepufferte Zitratlösung, pH 5,2.
Mitteilung Fa. Greiner 2011:
Die Lösungen selbst sind auf pH 5-6 gepuffert.
Mitteilung Fa. Roche Diagnostics 2011:
Roche Citrat-Pufferlösung pH 7,45 gepuffert.
Intra-Analytik
Mitteilung Fa. Terumo 2011:
Citrat-Citronensäure, pH 5,6 (bei Raumtemperatur) zur Erzielung eines finalen Blut-pH (9 + 1) zwischen 7,1 und 7,3 (bei Raumtemperatur).
Mitteilung Fa. Instrumentation Laboratory (IL) 2011:
Der pH Wert des HemosIL RecombiPlasTin Reagenz wird im normalen Bereich auf pH 7,3 - 7,5 mit einem TRIS-Puffer eingestellt.
Mitteilung Fa. Siemens 2011:
Das Reagenz Pathromtin SL enthält als Puffer ein Gemisch aus Hepes, Glycin, NaCl und EDTA, der pH Bereich liegt bei 7,5 bis 7,7. Der pH Wert des Reagenz-Plasma-Gemisches sollte ebenfalls zwischen 7,5 und 7,7 liegen.
Cave:
Terumo vs. IL vs. Siemens:
Ein pH im Reagenz-Plasma-Gemisch von 7,2 (Terumo) entspricht nach Meng et al. (2003) einer Gerinnungsaktivität von ca. 50 %, ein pH 7,3 - 7,5 (IL) einer von ca. 75 - 150 %, und ein pH von 7,6 (Siemens) einer von fast 200 %.
Die - hier geforderte - Standardisierung wird von anderer Seite (B. Pötzsch) aber strikt abgelehnt:
Kommentar zum Einsatz von Citrat-Pufferlösungen in der Gerinnungsdiagnostik
„Die Gewebstraumatisierung während der Blutabnahme und der Kontakt des Blutes mit den Fremdoberflächen aktiviert das Hämostasesystem partiell oder komplett bis zur Gerinnung. Um dies zu vermeiden, wird die Blutprobe bereits während der Blutabnahme mit einem Antikoagulationspuffer vermischt, um langfristig und dauerhaft eine Veränderung des Hämostaseprofils zu verhindern ohne die anschließende Gerinnungsanalytik zu beeinflussen. Diese Anforderungen werden von keinem der verfügbaren Antikoagulationspuffer vollständig erfüllt.
In der Routineanalytik etabliert sind gepufferte Citratlösungen. Durch eine Komplexbildung des Citrats mit freien Calciumionen im Blut wird der Gehalt an freiem Calcium im Blut soweit abgesenkt, dass die Calcium-abhängige Aktivierung des Hämostasesystems soweit minimiert wird, dass eine Lagerung des Blutes für einen begrenzten Zeitraum möglich wird, ohne das Hämostaseprofil relevant zu verändern. Durch Zugabe von exogenem Calcium zum Zeitpunkt der Gerinnungsanalytik ist der antikoagulatorische Effekt reversibel.
Die Stabilität von Gerinnungsfaktoren und Thrombozyten ist im leicht sauren Milieu höher. Deswegen werden in der Regel gepufferte Citratlösungen mit azidotischem pH-Wert eingesetzt. Die Stärke der pH-Wert-Erniedrigung ist abhängig von dem zu untersuchenden Analytspektrum.
Insgesamt sind die eingesetzten Blutabnahmesysteme und die Antikoagulationspuffer nicht getrennt von den analytischen Messverfahren zu betrachten, sondern als eine analytische Einheit zu beurteilen. Dementsprechend muss die Eignung jedes Antikoagulationssystems zur hämostaseologischen Diagnostik in Kombination mit dem jeweiligen Analysensystem überprüft werden.
Ein Antikoagulans, das für das gesamte Analytspektrum geeignet ist, existiert nicht. Darüber hinaus können Antikoagulationssysteme mit leicht abweichenden Zusammensetzungen eine vergleichbare Analysenqualität sicherstellen. Insofern ist es nicht sinnvoll einen Antikoagulationspuffer einheitlich zu definieren.“
Prof. Dr. B. Pötzsch, Institut für Experimentelle Hämatologie und Transfusionsmedizin, Universitätsklinikum Bonn
Generelles Fazit
- Die Gerinnungs-Aktivität der zu untersuchenden Probe ist sehr stark vom pH-Wert abhängig, eine Standardisierung ist daher unbedingt erforderlich. Eine Ablehnung oder eine Negierung dieser Problematik bedingt erhebliche diagnostische Fehler.
- Da eine Pufferung aller prä- und intra-analytischen Diagnostikschritte praktisch unmöglich ist, - welcher pH-Werte sollte denn der Probe in allen Fällen aufgezwungen werden -, wäre eine in allen Schritten gepufferte Diagnostik für den Patienten von großem Nachteil.
- Eine Standardisierung kann nur so erfolgen, dass der pH der Probe unverändert bleibt, das heißt, dass der ursprüngliche, in vivo-pH-Status der Probe gewahrt bleibt, um auch alle Azidose- oder Alkalose-bedingten Störungen des Gerinnungs-Status diagnostisch zu erfassen. Den ursprünglichen, in vivo-pH-Status der Probe zu erhalten, ist ein entscheidender Vorteil, am ehesten kann diese in vivo-Diagnostik des Patienten nur am point of care (POC) erfolgen.
- Aufforderung an die Hersteller von Blutentnahme-Systemen für Gerinnungs-Tests: Eine weitgehend gasdichte Blutgasspritze mit möglichst kleiner Gasblase sowie ungepuffertem Citrat in den Markt bringen.
Literatur
- Meng, ZH, Wolberg AS, Monroe DM, Hoffmann M: The effect of temperature and pH on the activity of factor VIIa: Implications for the efficacy of high-dose factor VIIa in hypothermic and acidotic patients. J Trauma 2003; 55: 886–891
- Polack B, Schved J-F, Boneu B: Preanalytical recommendations of the ´Groupe d´Etude sur l´hémostase et la thrombose´(GEHT) for venous blood testing in hemostasis laboratories. Haemostasis 2001; 31: 61-68
- Töpfer G, Lutze G, Sauer K et al.: Einfluß der Citratkonzentration im Blutentnahmeröhrchen auf hämostaseologische Meßgrößen. J Lab Med 2001; 25: 162-168
- Van Geest-Daalderop JHH, Mulder AB, Boonman-de Winter LJM et al.: Preanalytical variables and off-site blood collection: Influences on the results of the prothrombin time / international normalized ratio test and implications of monitoring of oral anticoagulant therapy. Clin Chem 2005; 51: 561-568
- Zander R, Lang W: Letter to the editor: Base Excess and strong ion difference: Clinical limitations related to inaccuracy. Anesthesiology 2004; 100:459–460
- Zander R: Forum Gerinnungsdiagnostik. Forum 2 – Citratlösungen (Präanalytik) (Ausgabe 03/2011)
